
2022-08-01 15:32:44來源:藥方舟瀏覽量:592
//
2011年12月,越洋醫藥從3個人、10平方米辦公室和30平方米實驗室起步。
2021年12月,越洋醫藥首款產品——左乙拉西坦緩釋片發貨美國,實現了產品“越洋”零的突破。
如今,越洋醫藥擁有7名全職歐美海歸博士、近200人的團隊,18個新藥獲批中國臨床試驗許可,12個新藥獲批美國臨床試驗許可。
//

7月31日,越洋醫藥舉行泰州成果轉化基地開工儀式。泰州醫藥高新區黨工委副書記、管委會主任,高港區委副書記、代區長丁志強出席儀式并致辭。
//

丁志強在致辭中表示,作為全國首個國家級醫藥高新區、全國唯一的部省共建醫藥高新區,中國醫藥城肩負著全省建設大健康產業集聚發展示范區的重要使命,正搶抓市委市政府“舉全市之力建設中國醫藥城”的戰略機遇,全力打造改革先行區、創新活力區、發展引領區、幸福示范區。
醫藥高新區將始終秉持“專業、專注、專心”的工作理念,一如既往地關心、支持項目建設,堅定不移地為項目建設和企業發展提供最優質、最便捷、最高效的服務,著力營造重商、安商、親商的濃厚氛圍,讓項目盡快全面建成投產,讓企業不斷發展壯大。
//

越洋醫藥董事長聞曉光博士致辭暨成果發布
//

越洋醫藥股東、戰略合作伙伴代表李靜文發言
//

泰州醫藥高新區黨工委副書記、管委會主任,高港區委副書記、代區長丁志強;越洋醫藥董事長聞曉光;揚子江藥業集團有限公司黨委書記、董事長、總經理徐浩宇;招商銀行股份有限公司泰州分行行長徐一;高港區政府副區長施康振;上海醫藥技術創新中心助理主任李靜文;泰州醫藥產業園管理辦公室黨工委副書記、主任吳翔共同啟動開工儀式。
企業名片

“我們越洋留學讀書,又越洋回來創業,將來還要讓我們的新藥產品越洋銷售全球。因此,公司起名越洋醫藥。”聞曉光博士說。如今,他做到了,并且會越來越好。
2011年12月,聞曉光博士在中國醫藥城創辦泰州越洋醫藥開發有限公司,專注于應用自主創新和通用緩控釋平臺技術,開發適應美國(NDA/505(b)(2))、中國(化藥2類)及全球市場的新藥。
2020年12月,越洋醫藥完成3.3億元C輪融資,投資方為上海醫藥、華美國際集團、乾道集團。
2021年12月,越洋醫藥成功舉行了左乙拉西坦緩釋片出口美國的首次發貨儀式,實現了產品“越洋”零的突破。
如今,越洋醫藥擁有7名全職歐美海歸博士、近200人的團隊,18個新藥獲批中國臨床試驗許可,12個新藥獲批美國臨床試驗許可。其中,新藥“維安”在美國等地開展500多名患者的國際多中心III期臨床試驗。由于越洋醫藥2類創新藥的開發處于領先地位,被中國化學制藥工業協會推薦為二類新藥專委會主任單位。
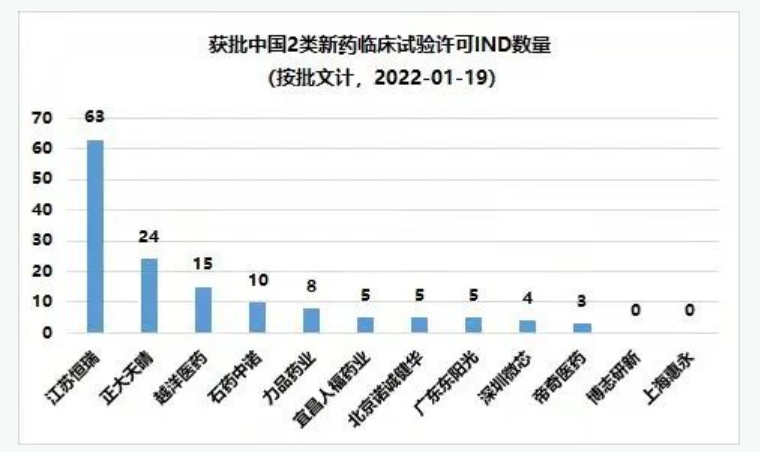
二類新藥臨床批件數量全國第三

緩控釋新藥臨床批件數量全國第一
創始人介紹

聞曉光博士是越洋醫藥創始人兼任董事長,國家級特聘專家,北大醫學部優秀校友,化學制藥工業協會二類新藥專委會主任委員,藥學會制劑專業委員會委員,藥學會工業藥劑學專委會委員,中國顆粒協會理事,是《Oral Controlled Release Formulation Design and Drug Delivery:Theory to Practice》一書以及綜述《新型制劑的研發與創新》【科技導報2016, 34(11)】的作者之一。
聞曉光博士回國前曾在GSK和Pfizer從事緩控釋制劑新藥開發多年,曾參與多個原創制劑新藥的開發。國家科技部制劑新技術國家重點實驗室主任(揚子江藥業承載)。17項緩控釋技術和產品獲得中美歐日發明專利授權。
擬稿:冀綱
審核:居斌
發布:冀綱
聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!