
2023-05-06 15:08:21來源:藥方舟瀏覽量:346
2023年4月14-19日,美國癌癥研究協(xié)會(AACR)年會在美國佛羅里達(dá)州奧蘭多召開。作為全球范圍內(nèi)備受矚目的癌癥研究會議,大會上發(fā)布了諸多癌癥領(lǐng)域的重磅研究結(jié)果,吸引行業(yè)的關(guān)注。近期,醫(yī)藥地理pro將發(fā)布一系列此次AACR大會上發(fā)表的重磅研究,供醫(yī)藥同仁參考。

Allogene在AACR上以口頭報告的形式展示了其自研CAR T療法ALLO-316的Ⅰ期TRAVERSE試驗的中期數(shù)據(jù),該試驗療法是該公司第一個用于實體瘤的同種異體嵌合抗原受體T細(xì)胞(AlloCAR TTM)候選研究產(chǎn)品。研究數(shù)據(jù)表明,ALLO-316顯示出早期的抗腫瘤活性,并隨著時間的推移不斷加深,AlloCAR T有可能治療表達(dá)CD70的晚期或轉(zhuǎn)移性腎細(xì)胞癌(RCC)患者。
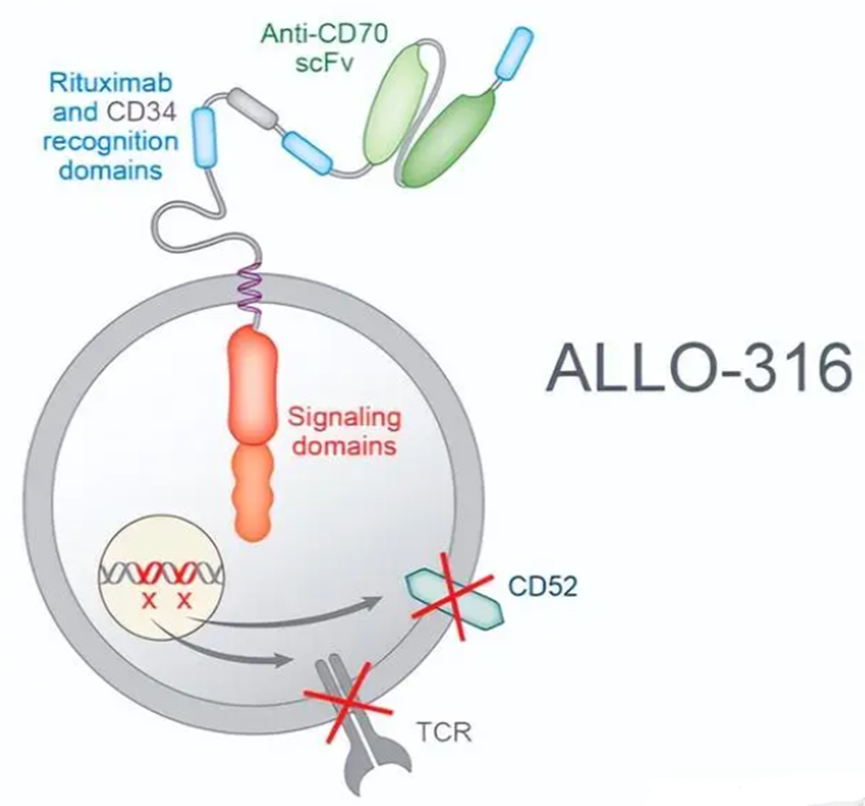
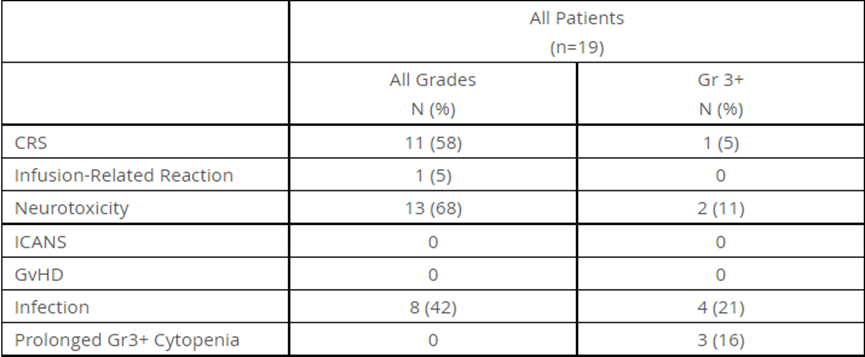
試驗旨在評估ALLO-316對晚期或轉(zhuǎn)移性腎細(xì)胞癌患者的安全性、耐受性和活性。數(shù)據(jù)顯示,在18名可評估療效的患者中,其疾病控制率(DCR)為89%。在已知表達(dá)CD70的10名患者中,其疾病控制率為100%,3名患者獲得部分緩解(2名確認(rèn),1名未確認(rèn))。最長的反應(yīng)時間持續(xù)到第八個月。在CD70表達(dá)水平較高的患者中,腫瘤表現(xiàn)出縮小的趨勢。在19名可評估療效的患者中,到目前為止,ALLO-316表現(xiàn)出與自體CAR T療法基本一致的不良事件。

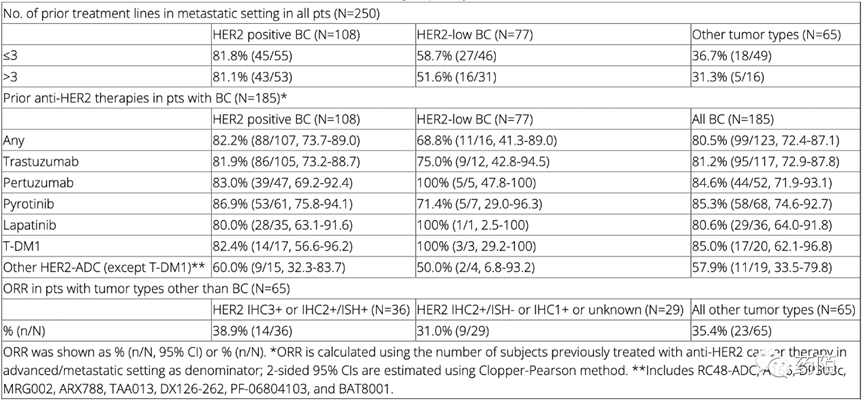
本屆aacr大會發(fā)布了A1811對HER2 陽性/突變實體的I期數(shù)據(jù)。研究納入標(biāo)準(zhǔn)治療無效或不耐受的HER2陽性乳腺癌、HER2陽性胃/GEJ癌、HER2低表達(dá)乳腺癌、HER2表達(dá)/突變型NSCLC或其他HER2表達(dá)/突變型實體瘤患者。SHR-A1811劑量為1.0 ~ 8.0 mg/kg,每3周給藥。
結(jié)果顯示,250 例既往接受過中位3線治療的轉(zhuǎn)移性乳腺癌患者接受了劑量遞增、PK擴(kuò)展,有1例患者經(jīng)歷了DLT。TRAE發(fā)生率97.2%,≥3級TRAE發(fā)生率52.4%、嚴(yán) 重TRAE發(fā)生率12.4%, 治療相關(guān)死亡3例(1.2%), 8例(3.2%)患者報告了ILD。總ORR為61.6% (154/250, 95% CI 55.3 ~ 67.7),HER2陽性乳腺癌 ORR 81.5% (88/108,95% CI 72.9 ~ 88.3)、HER2低表達(dá)乳腺癌ORR 55.8% (43/77, 95% CI 44.1 ~ 67.2)、尿路上皮癌ORR 63.6% (7/11)、 結(jié)直腸癌ORR 30% (3/10)、胃GEJ癌ORR 55% (5/9)、膽道癌62.5% (5/8)、非小細(xì)胞肺癌(NSCLC) (1/3)、子宮內(nèi)膜癌(1/2) 和H&N癌(1/1)患者均 觀察到客觀緩解。全組6個月PFS率為73.9%。
文章版權(quán)歸原作者所有。如涉及作品內(nèi)容、版權(quán)和其它問題,請跟我們聯(lián)系刪除!文章內(nèi)容為作者個人觀點,并不代表本平臺贊同或支持其觀點。本平臺擁有對此聲明的最終解釋權(quán)。