
2020-08-17 11:58:24來源:藥智網瀏覽量:687
第三批集采就要在8月20日開標,“集采入場券”一致性評價工作仍在有條不紊的進行中,截至8月14日,CDE受理一致性評價受理號累計2289個(592個企業的535個品種,按補充申請計,下同);其中已有661個受理號過評。本周(8月7日至8月14日),又有5個品種過評,多個超10億級大品種在列;還有13個品種獲承辦...
過評詳情
5個品種過評;10億級「索拉非尼」首仿獲批
本周有7個品規(5個品種)通過一致性評價,其中3個品種視同過評,2個為批準補充,且江西山香藥業的甲苯磺酸索拉非尼片為國內首仿,具體詳情如下:
本周一致性評價過評詳情表
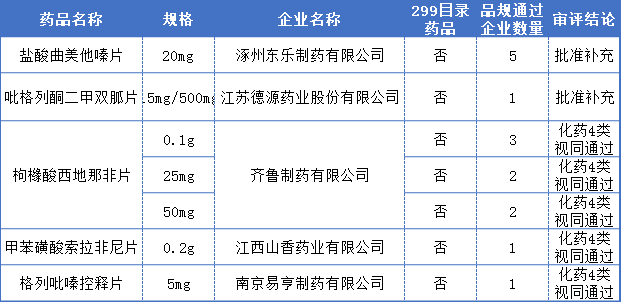
鹽酸曲美他嗪片
鹽酸曲美他嗪是第一個3-酮酰輔酶A硫解酶(3-KAT)抑制劑類代謝制劑,作為添加藥物,用于對一線抗心絞痛治療控制不佳或無法耐受的穩定型心絞痛成年患者的對癥治療。其原研企業為施維雅,最早在法國上市,2000年中國獲批進口。
據藥智數據,我國現有鹽酸曲美他嗪片市場批文10條,包括原研企業在內,涉及生產廠家10家;2019年國內樣本醫院銷售額為4.78億元,其中超70%的份額為被原研企業占據,其次是瑞陽制藥13.09%,本周過評的涿州東樂制藥沒有在銷售TOP10之內。
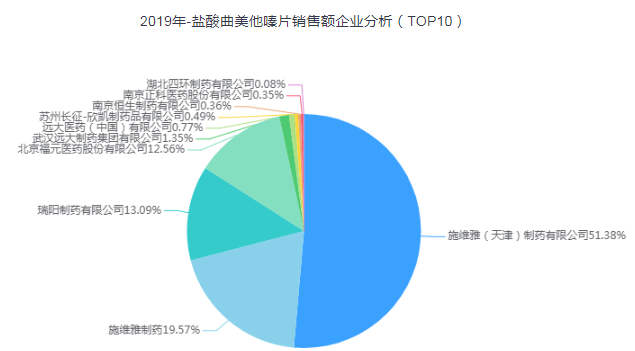
截至目前,鹽酸曲美他嗪片累積已有5家通過一致性評價,分別是涿州東樂制藥、瑞陽制藥、遠大醫藥、北京萬生、江蘇吳中、蘇州制藥廠。
吡格列酮二甲雙胍片
吡格列酮二甲雙胍片(復瑞彤)是吡格列酮和二甲雙胍組成的復方制劑,用于治療2型糖尿病。
據藥智數據,我國現僅有江蘇德源藥業和杭州中美華東制藥兩家企業擁有該復方制劑市場批文;中國藥學會樣本醫院數據(CPA數據)顯示:2019年國內吡格列酮二甲雙胍樣本醫院總體銷售額約9016萬元,江蘇德源藥業該產品樣本市場占比6.79%;2020年一季度國內吡格列酮二甲雙胍樣本醫院總體銷售額約2279萬元,江蘇德源藥業“復瑞彤”樣本市場占比8.84%。樣本市場銷售額及占比均呈上升趨勢。
另據藥智網一致性評價進度數據庫顯示,江蘇德源藥業首家通過一致性評價,有望提升該藥品的市場競爭力,為其將來銷售增長奠定堅實的基礎。
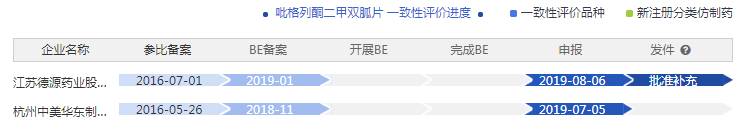
枸櫞酸西地那非片
枸櫞酸西地那非片為5型磷酸二酯酶(PDE-5)抑制劑,用于治療罕見病成人肺動脈高壓(PAH,WHO第1組),以改善運動能力和延緩臨床惡化。西地那非的原研企業為輝瑞,FDA于1998年3月27日批準其上市,成為首個治療ED的磷酸二酯酶-5(PDE-5)抑制劑為ED一線用藥。
網絡公開數據顯示,2019年中國城市零售藥店終端西地那非銷售額超過23億元,白云山市場份額占比第一,其次為原研企業輝瑞。
截止目前,枸櫞酸西地那非片國產市場批文有13條,生產廠家7家,其中3個企業的3個品規已經通過一致性評價,本周齊魯制藥該品種按新化藥4類注冊獲批,視同過評,向20億級的抗ED市場發起挑戰。
枸櫞酸西地那非片一致性評價過評詳情表

另值得提及的是枸櫞酸西地那非片為第三批集采目錄藥品,齊魯制藥在即將開標之際,獲批上市,來得早不如來得巧,正好搭上第三批集采的順風車,形成3+1的競標格局。
甲苯磺酸索拉非尼片
索拉非尼是一款口服多靶點、多激酶抑制劑。臨床上主要用于治療肝細胞癌、腎細胞癌和甲狀腺癌。索拉非尼由拜耳研制,2005年12月獲得FDA批準上市,2006年8月在中國獲批,2017年通過國家談判納入醫保乙類目錄并在2019年再次降價成功續約。目前,國內醫保支付標準為95元/片。
據悉,2019年,索拉非尼國內銷售額約12億元,其中樣本醫院銷售額達6.6億元,截止目前國內甲苯磺酸索拉非尼片仿制藥申報上市的僅4家企業,山香藥業一馬當先,奪得首仿的同時視同通過一致性評價,打破原研壁壘。
甲苯磺酸索拉非尼片仿制藥報產詳情表
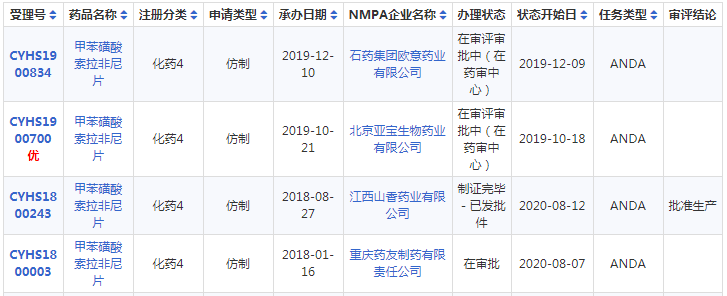
格列吡嗪控釋片
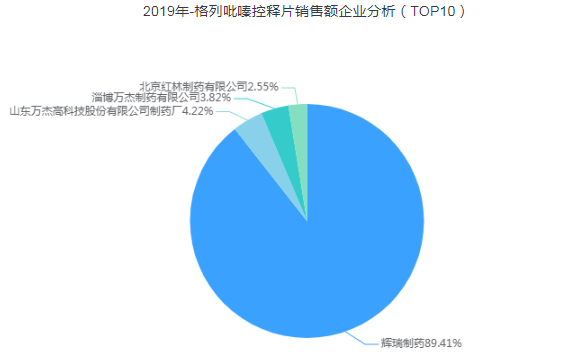
格列吡嗪是一種磺脲類降糖藥,由輝瑞開發;國內生產銷售的劑型有片劑、分散片、口崩片、緩釋片、控釋片和膠囊劑等。據藥智數據顯示,其中控釋片僅淄博萬杰制藥、北京紅林制藥、常州四藥制藥、以及剛獲批的南京易亨制藥4家國產企業獲批生產。
2019年格列吡嗪控釋片樣本醫院銷售額為1.20億元,其中原研輝瑞占據絕大部分份額,達89.41%。現除南京易亨制藥首家視同通過一致性評價外,暫無其他企業過評,能否借此機會搶占原研份額,拭目以待。
申報受理
13個品種被承辦,恒瑞核心首仿造影劑再獲受理
本周CDE新增一致性評價受理號20個(13個品種),注射劑再次搶眼,有8個品種申報一致性評價被承辦,恒瑞、倍特、石藥中諾、羅欣等知名企業的重磅產品紛紛在列。
本周一致性評價申報受理詳情
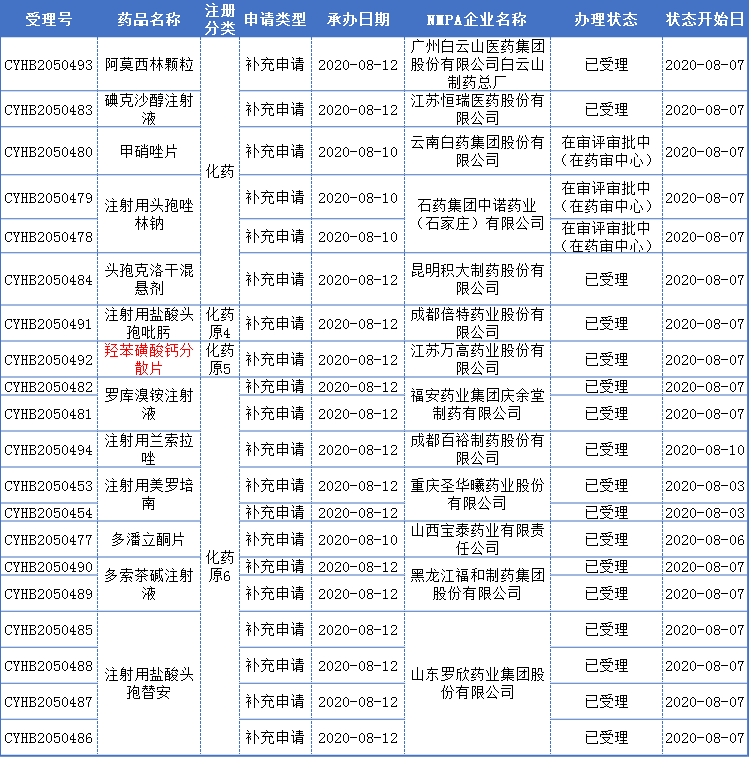
注:紅的標注為本周首家申報受理品種
其中值得提及的是恒瑞醫藥的碘克沙醇注射液,碘克沙醇注射液是X-線對比劑,主要用于成人心血管造影、腦血管造影、外周動脈造影、腹部血管造影、尿路造影、靜脈造影以及CT增強檢查、兒童心血管造影。
恒瑞醫藥碘克沙醇注射液為國內首仿產品,且為恒瑞醫藥核心造影劑產品之一,中國醫藥工業信息中心的數據顯示,2019年國內碘克沙醇市場規模為49.71億元,占整個造影劑市場份額的35.65%。另據企業公告,2019年恒瑞造影劑實現營收32.3億元,同比增長近39%,國內造影劑市占率排第一。
此前,恒瑞醫藥碘克沙醇注射液已有2個受理號申報一致性評價其中一個辦理狀態呈“已發件”狀態,現又一受理號獲受理,能否再次在首仿的基礎之上搶先通過一致性評價,鞏固首仿地位,獲得更大造影劑市場蛋糕,可期可待。
碘克沙醇注射液一致性評價申報受理詳情表

聲明:本文系藥方舟轉載內容,版權歸原作者所有,轉載目的在于傳遞更多信息,并不代表本平臺觀點。如涉及作品內容、版權和其它問題,請與本網站留言聯系,我們將在第一時間刪除內容!