
2023-12-29 00:00:00來源:Cancer Research Communications瀏覽量:188
人類的三個Ras基因,HRAS、KRAS和NRAS,在三分之一的人類癌癥中頻繁發生突變,其中KRAS突變是三個亞型中最為普遍的(約86%的病例)。由于KRAS的高突變頻率以及其在推動人類腫瘤發生和對癌癥治療的抵抗中的關鍵作用,我們迫切需要尋找能夠抑制突變型(mt)KRAS的藥物。
?
?
隨著科學技術的不斷突破,我們已經發現了可與 mt KRAS G12C 形成共價結合的小分子,例如?sotorasib?和?adagrasib,這些藥物已被用于治療攜帶 KRAS G12C 突變的晚期非小細胞肺癌(NSCLC)患者。此外,我們還發現了能夠結合 KRAS G12D 的?MRTX1133。然而,目前仍然沒有臨床批準的用于治療 KRAS G12D 突變的藥物(MRTX1133詳情可見往期:TargetMol明星分子——MRTX1133)。
?
近日,一項發表于?Cancer Research Communications?的研究給我們帶來了驚喜,來自 VCU 梅西綜合癌癥中心的研究團隊發現了可靶向 KRAS G12D 的新型藥物 KRB-456,能夠有效阻止攜帶 mt KRAS G12D 和 G12V 的胰腺癌患者在化療和放療后復發后的皮下和異種移植瘤的體內生長,有望走向臨床。
▲點擊圖片可跳轉原文
?
發現KRB-456
在最新研究中,為了尋找能夠結合 mt KRAS G12D 的小分子,研究人員首先使用 AlphaScreen 篩選出了能夠干擾?KRAS G12D 與?RAF1 的 RBD(RAS結合結構域)結合的化合物。其中有6個(IB-21G、IB-21L、IIA-15D、IB-21J、IB-5I 和 IIA-13L)顯著抑制了 GTP-KRAS G12D 與 GST-RBD 的結合(77%?至?100%?的抑制)。
?
在這 6 個化合物中,有 4 個(IB-21G、IB-21L、IIA-15D 和 IB-21J)共享相同的藥效團,在抑制 KRAS G12D 與 GST-RBD 結合方面最為有效(98%至100%的抑制)。另外兩個化合物,IB-5I 和 IIA-13L,具有不同的藥效團,分別為 89% 和 77% 的抑制率。

▲KRB-456的篩選
?
進一步的 GST pull-down 分析顯示,化合物 IB-21L(以下簡稱為KRB-456)是抑制 KRAS G12D/GST-RBD 相互作用最有效的化合物,IC50 值為 260 nM。

▲GST pull-down 分析結果
?
為更好地了解 KRB-456 與 KRAS G12D 的結合相互作用,研究人員進行了 2D 1H-15N 異核單量子相干(HSQC)NMR 分析,使用 15N 標記的 KRAS G12D 結合 GDP 和不可水解的 GTP 核苷酸類似物 GCP(β,γ-Methyleneguanosine 5′-triphosphate)。結果顯示?KRB-456 通過與 switch-I/II 區域內的一個動態變構結合口袋形成相互作用來結合 KRAS G12D。
?
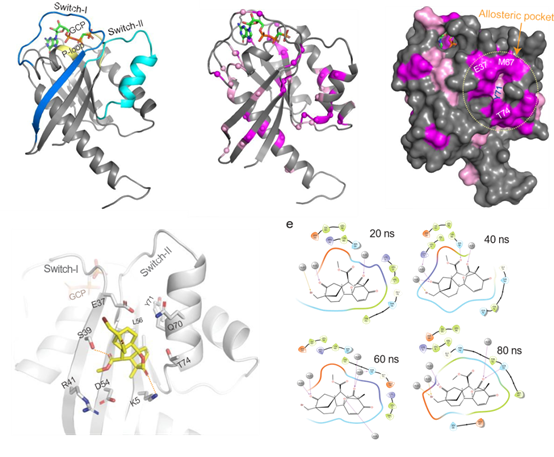
▲KRB-456與KRAS G12D的結合
?
接下來,研究人員通過使用4名胰腺癌患者的新鮮活檢組織確定了 KRB-456 是否能夠抑制小鼠中患者源異種移植物(PDX)的生長,其中 3 名患者(G166、G148 和 G160)的腫瘤攜帶 KRAS G12D 突變,另一名患者(G174)的腫瘤攜帶 KRAS G12V 突變。
通過將所有 4 名患者的新鮮切除的腫瘤活檢皮下(s.c.)植入 NSG 小鼠,并將隨即小鼠分為對照組和 KRB-456 組。結果顯示,在所有 KRB-456 處理的小鼠中,腫瘤生長在治療的第 3 天就被顯著抑制,到 KRB-456 藥物治療結束時,平均生長僅為52%、177%、300% 和 413%,相比之下,對照組分別為 401%、433%、802%和 791%。KRB-456 顯著抑制了胰腺癌患者 PDX 在小鼠皮下植入的腫瘤生長。
進一步,研究人員將患者 G160 的腫瘤活檢在 NSG 小鼠中原位植入來確定 KRB-456 是否也能抑制原位腫瘤模型的生長(G160在原位植入時生長速度比皮下植入慢得多)。在腫瘤植入 20 天后,小鼠每天用 KRB-456 進行腹腔注射治療 ,發現?KRB-456 治療抑制了患者 G160 原位植入的PDX的生長。證明了 KRB-456 不僅在皮下 PDX 腫瘤生長中有效,而且在源自胰腺癌患者的腫瘤原位生長中也有效,KRB-456 以劑量依賴的方式抑制了這些胰腺癌細胞的生存能力,抑制效果可達到 70%。
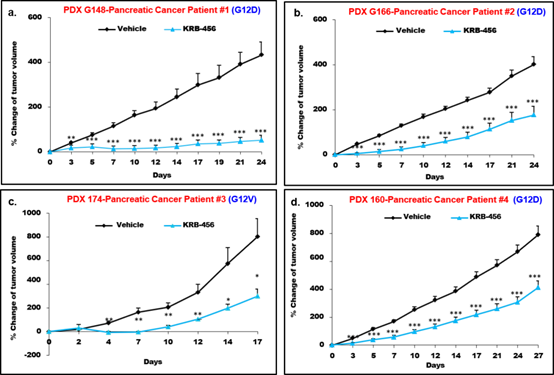
▲KRB-456 對腫瘤的抑制效果
?
此外, 3D 共培養模型顯示,當患者來源的腫瘤細胞單獨培養或與促進化療抵抗的人類胰腺星形細胞共培養時,KRB-456 仍然能以劑量依賴的方式顯著抑制這些胰腺癌細胞的生存能力。
?
?
總結
綜上,該研究首次發現了一種名為 KRB-456 的新型小分子,它能夠與 KRAS G12D 形成高親和力結合,通過作用于 KRAS 蛋白的動態異構性結合口袋,抑制其與 RAF1 的結合,從而有效阻斷胰腺癌細胞的 KRAS G12D 介導的腫瘤生長。
KRB-456 在體外和體內研究中表現出優越的抗腫瘤活性,不僅能夠顯著減少 GTP 結合的 KRAS 水平,還能抑制 P-MEK 的活性,引起細胞凋亡。實驗證明 KRB-456 對攜帶 KRAS G12D 和 KRAS G12V 突變的胰腺癌病人源腫瘤模型均具有顯著的抑制效果,尤其對于那些經過化療和放療后復發的患者的腫瘤生長,顯示出潛在的克服藥物耐受性的能力。此外,KRB-456 在 3D 共培養模型中顯示出對胰腺癌患者源腫瘤細胞的顯著抗活性,為該分子在克服化療和放療耐受性方面的臨床應用提供了重要線索。總體而言,這項研究為尋找更廣泛的 KRAS 突變型抑制劑提供了新思路,尤其是針對 KRAS G12D 和 KRAS G12V,為治療胰腺癌等高發癌癥開辟了新的治療途徑。
?
此外,該研究中提到的化合物sotorasib?、adagrasib和?MRTX1133?等 TargetMol?都可以提供噢,還有?抗胰腺癌化合物庫、抗腫瘤篩選化合物庫?等可供選擇,有任何問題歡迎私信咨詢~
?
原文文獻:
Kazi A, Ranjan A, Kumar M V V, et al. Discovery of KRB-456, a KRAS G12D switch-I/II allosteric pocket binder that inhibits the growth of pancreatic cancer patient-derived tumors. Cancer Res Commun. Published online December 5, 2023. doi:10.1158/2767-9764.CRC-23-0222
?