
2024-04-15 00:00:00來源:陶術(shù)生物瀏覽量:188
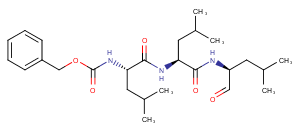
MG-132貨號T2154,別名?Z-LLL-al,Z-Leu-Leu-Leu-CHO。MG-132是一種 26S 蛋白酶體抑制劑 (IC50=100 nM),具有細(xì)胞滲透性、可逆性。 MG-132可誘導(dǎo)凋亡。
 ?
?
圖??MG-132分子結(jié)構(gòu)式
1.?背景介紹
26S蛋白酶體是細(xì)胞內(nèi)最重要的蛋白質(zhì)降解系統(tǒng)之一,也稱為泛素-蛋白酶體系統(tǒng)(UPS,Ubiquitin-Proteasome System)。這個系統(tǒng)主要由兩個部分組成:泛素化系統(tǒng)和蛋白酶體。
泛素化系統(tǒng):這一系統(tǒng)涉及將泛素分子共價(jià)結(jié)合到目標(biāo)蛋白質(zhì)上,標(biāo)記這些蛋白質(zhì)為需要降解的目標(biāo)。這個過程涉及泛素激活酶、泛素連接酶和泛素連接酶,它們共同將泛素連接到特定的蛋白質(zhì)上形成多泛素鏈。
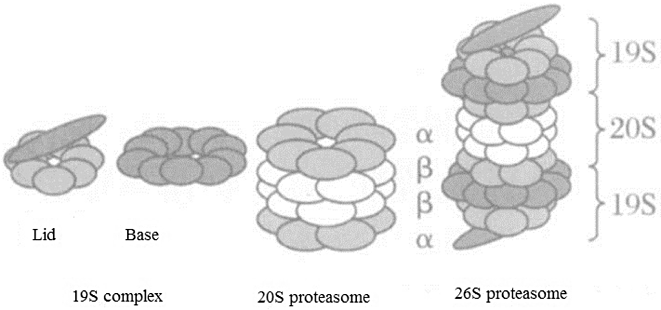
蛋白酶體:這個系統(tǒng)主要由20S核心粒子和與其結(jié)合的19S調(diào)節(jié)粒子組成,形成26S的復(fù)合物。26S蛋白酶體是負(fù)責(zé)降解已被泛素標(biāo)記的蛋白質(zhì)的主要細(xì)胞內(nèi)蛋白酶體。它通過識別、解構(gòu)和降解已泛素化的蛋白質(zhì),從而起到維持細(xì)胞內(nèi)蛋白質(zhì)質(zhì)量和調(diào)節(jié)蛋白水平的重要作用。
 ?
?
圖 ?蛋白酶體結(jié)構(gòu)示意圖
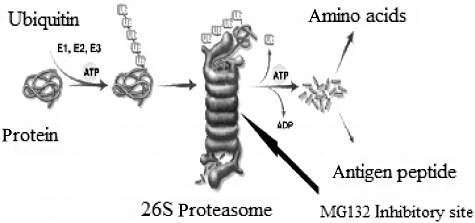
26S蛋白酶體可以維持細(xì)胞內(nèi)蛋白質(zhì)的穩(wěn)態(tài),通過清除異常、老化或過多的蛋白質(zhì),參與調(diào)控細(xì)胞生命周期、應(yīng)激應(yīng)答和代謝調(diào)節(jié)等生理過程。MG-132作為26S蛋白酶體的抑制劑,能夠干擾這一系統(tǒng)的正常功能,為研究細(xì)胞生物學(xué)和分子生物學(xué)提供重要工具和信息。此外,癌細(xì)胞凋亡與泛素-蛋白酶體通路的活性密切相關(guān)。MG132可以通過不同的中間途徑誘導(dǎo)細(xì)胞凋亡,在抗腫瘤治療中起著至關(guān)重要的作用[1]。
 ?
?
圖?MG132的抑制途徑
?
3. 應(yīng)用文獻(xiàn)精選
3.1文章標(biāo)題:Brusatol induces ferroptosis in oesophageal squamous cell carcinoma by repressing GSH synthesis and increasing the labile iron pool via inhibition of the NRF2 pathway
 ?
?
研究概覽:本文研究發(fā)現(xiàn)一種在 Brucea sumatrana 中發(fā)現(xiàn)的生物活性化合物Brusatol(Bru),對多種惡性腫瘤具有抗腫瘤作用。在研究其作用機(jī)制的過程中發(fā)現(xiàn)Bru是通過抑制 GSH 合成并通過抑制 NRF2 通路增加不穩(wěn)定的鐵庫來誘導(dǎo)食管鱗狀細(xì)胞癌的鐵死亡,即Brusatol通過鐵死亡發(fā)揮抗腫瘤活性[2]。
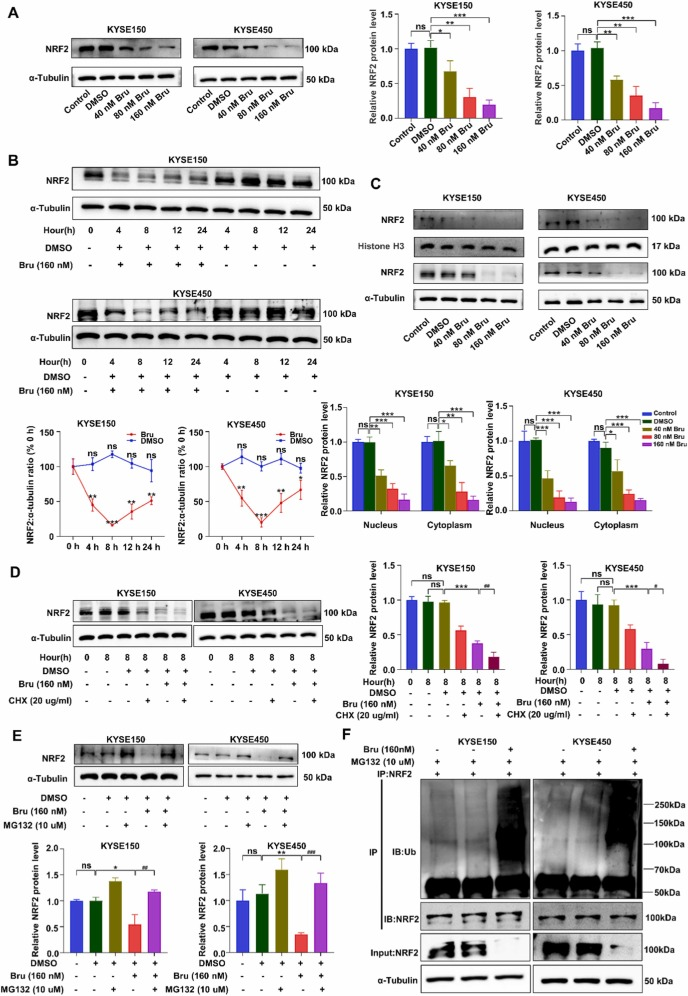
本文實(shí)驗(yàn)中使用Bru處理KYSE150 和 KYSE450 細(xì)胞加速了NRF2的泛素化和降解,抑制了NRF2的生物活性,從而導(dǎo)致鐵死亡的啟動。實(shí)驗(yàn)過程中使用10μM的MG-132處理細(xì)胞(2小時)可以減輕Bru誘導(dǎo)的NRF2的泛素化和降解(如下圖)。
 ?
?
圖??Bru 通過泛素-蛋白酶體途徑促進(jìn) NRF2 降解
?
3.2文章標(biāo)題:Deubiquitinase OTUD6A in macrophages promotes intestinal inflammation and colitis via deubiquitination of NLRP3
 ?
?
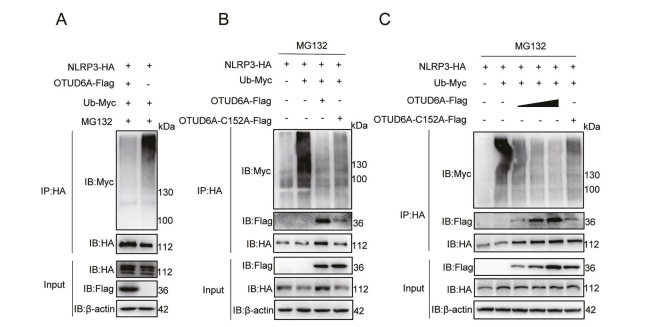
研究概覽:本文研究發(fā)現(xiàn)巨噬細(xì)胞中的去泛素化酶?OTUD6A 通過 NLRP3 的去泛素化促進(jìn)腸道炎癥和結(jié)腸炎。在研究其作用機(jī)制過程中發(fā)現(xiàn)OTUD6A 直接與 NLRP3 炎癥小體的 NACHT 結(jié)構(gòu)域結(jié)合,并在 K430 和 K689 位點(diǎn)選擇性地從 NLRP3 中切割 K48 連接的多泛素鏈以增強(qiáng) NLRP3 的穩(wěn)定性,導(dǎo)致 IL-1β 水平升高和炎癥。總之,本文研究團(tuán)隊(duì)發(fā)現(xiàn)通過促進(jìn)NLRP3炎癥小體激活,確定了OTUD6A在結(jié)腸炎發(fā)病機(jī)制中的新功能,表明OTUD6A可能是治療炎癥性腸病(IBD)的潛在靶點(diǎn)[3]。
本文研究OTUD6A調(diào)控NLRP3活性的分子機(jī)制時,發(fā)現(xiàn)OTUD6A直接去泛素化NLRP3,抑制其蛋白酶體降解,提高其穩(wěn)定性和水平。在細(xì)胞實(shí)驗(yàn)中使用含有10μM的MG-132處理細(xì)胞(6小時),發(fā)現(xiàn)MG-132可以抑制NLRP3蛋白的表達(dá)。
 ?
?
圖 ?OTUD6A去泛素化NLRP3
3.3文章標(biāo)題:The SARS-CoV-2 papain-like protease suppresses type I interferon responses by deubiquitinating STING
 ?
?
研究概覽:本文研究團(tuán)隊(duì)發(fā)現(xiàn)SARS-CoV-2 木瓜蛋白酶樣蛋白酶(PLpro)通過去泛素化 STING 來抑制 I 型干擾素反應(yīng),并研究了PLpro拮抗細(xì)胞抗病毒反應(yīng)的機(jī)制[4]。
本文研究在進(jìn)行去泛素化實(shí)驗(yàn)時使用蛋白酶體抑制劑10 μM 的MG-132 處理細(xì)胞(4小時)。
 ?
?
圖 ?SARS-CoV-2 plpro介導(dǎo)的IFN-I應(yīng)答拮抗模型
?
參考文獻(xiàn)
[1] Guo N, Peng Z. MG132, a proteasome inhibitor, induces apoptosis in tumor cells. Asia Pac J Clin Oncol. 2013;9(1):6-11. doi:10.1111/j.1743-7563.2012.01535.x
[2]?Zhu X, Huang N, Ji Y, Sheng X, Huo J, Zhu Y, Huang M, He W, Ma J. Brusatol induces ferroptosis in oesophageal squamous cell carcinoma by repressing GSH synthesis and increasing the labile iron pool via inhibition of the NRF2 pathway. Biomed Pharmacother. 2023 Nov;167:115567. doi: 10.1016/j.biopha.2023.115567. Epub 2023 Sep 22. PMID: 37742602..
[3]?Liu X, Fang Y, Lv X, et al. Deubiquitinase OTUD6A in macrophages promotes intestinal inflammation and colitis via deubiquitination of NLRP3. Cell Death Differ. 2023;30(6):1457-1471. doi:10.1038/s41418-023-01148-7
[4] Cao D, Duan L, Huang B, Xiong Y, Zhang G, Huang H. The SARS-CoV-2 papain-like protease suppresses type I interferon responses by deubiquitinating STING. Sci Signal. 2023 May 2;16(783):eadd0082. doi: 10.1126/scisignal.add0082. Epub 2023 May 2. PMID: 37130168.
?